Candida auris, een schimmel die aan een wereldwijde opmars bezig is, blijkt multiresistent te zijn. Het gevaar voor een nieuwe epidemie neemt toe.
Weer actueel. Dit artikel verscheen eerder in Eos (september 2021). Het is opnieuw actueel nu de Wereldgezondheidsorganisatie waarschuwt voor de ‘groeiende dreiging’ van resistente schimmels. Vooral de schimmel Candida auris baart de WHO zorgen.
Het is intussen veertien jaar geleden sinds Japanse onderzoekers een schimmel isoleerden uit het oor van een zeventigjarige vrouw in Tokio. Het ging om een nieuwe soort, die Candida auris werd gedoopt – naar het Latijnse auris voor ‘oor’.
Vandaag staat de schimmel bekend om zijn extreme resistentie, zijn supersnelle verspreiding en het hoge sterftecijfer van patiënten die ermee besmet raken. In de Verenigde Staten heeft het federale Center for Disease Control (CDC) de schimmel opgenomen in zijn lijst met meest alarmerende resistente microbes ter wereld. C. auris is de eerste schimmel ooit op die lijst.
Dat alles – samen met zijn onbekende oorsprong – maken van C. auris een mysterieuze superschimmel. Waar komt hij vandaan, hoe komt het dat hij zo gevaarlijk is en wat kunnen we eraan doen? Wetenschappers zoeken naar antwoorden. En daar zit wel wat haast achter.
Verspreiding onder de radar
Nadat C. auris bij de Japanse vrouw voor het eerst beschreven werd, bleef het even stil rond de schimmel. De oorinfectie was niet levensbedreigend. Bovendien maken wetenschappers jaarlijks melding van heel wat nieuwe micro-organismen, meestal afkomstig uit de natuur maar soms ook uit infecties van dieren en mensen. C. auris viel niet meteen op en verdween van de radar.
Vier jaar later, in 2011, werd de schimmel voor het eerst gevonden in het bloed van drie erg zieke patiënten in Zuid-Korea. Twee daarvan overleden na behandeling. In de daaropvolgende jaren volgden steeds meer rapporteringen van zeldzame schimmelinfecties, zoals van Saccharomyces cerevisiae, Candida haemulonii en Rhodotorula glutinis. Artsen hadden de schimmels aangetroffen in het bloed van patiënten in India, China, Pakistan, Colombia, Venezuela, Kenia en Zuid-Afrika. Later bleek het te gaan om misdiagnose: in werkelijkheid ging het telkens om C. auris-infecties.

Geleidelijk aan begon het wetenschappers te dagen dat deze schimmel heel wat agressiever is dan ze aanvankelijk hadden gedacht. Uit rapporten bleek dat het mortaliteitscijfer van C. auris hoog was: 30 tot 60 procent van de patiënten sterft aan de gevolgen van de infectie.
Reden genoeg voor het Europees Centrum voor ziektepreventie en -bestrijding (ECDC) om aan de alarmbel te trekken. Zes Europese landen, waaronder België, werden opgeroepen om in hun databanken na te gaan of ze C. auris al eerder hadden geïsoleerd maar vervolgens verkeerd hadden geïdentificeerd. Uit het onderzoek bleek Candida auris tussen 2013 en 2017 uit maar liefst 620 patiënten te zijn geïsoleerd: 388 in Spanje, 221 in het Verenigd Koninkrijk, zeven in Duitsland, twee in Frankrijk, en telkens één in Noorwegen en België.
Ook de Verenigde Staten bleven niet gespaard. Artsen rapporteerden er meer dan 1.500 infecties, met dodelijke uitbraken in ziekenhuizen in de staten New York, Illinois en California. In 2018 dook de schimmel ook in Australië op – sinds dat moment is C. auris aanwezig op elk continent behalve Antarctica.
Sinds 2018 is C. auris aanwezig op elk continent behalve Antarctica
Het zette wetenschappers aan het denken: zou C. auris wel echt zo nieuw zijn? Om na te gaan of er in het verleden niet nog meer infecties met C. auris verkeerd waren gediagnosticeerd, begonnen artsen in ziekenhuizen over de hele wereld de schimmelisolaten van jaren geleden opnieuw te onderzoeken. Daaruit bleek dat de vroegste C. auris-infecties teruggaan tot 1996. Toch is het intussen duidelijk dat deze superschimmel zich pas in de laatste tien jaar werkelijk heeft verspreid. Hoe kan dat?
Van moeras naar ziekenhuis
Wetenschappers analyseerden de verwantschap van honderden C. auris-isolaten van over de hele wereld door hun DNA te vergelijken. Ze kwamen tot een verbluffende vaststelling: de schimmel is gelijktijdig opgedoken op verschillende continenten. Door de stamboom van de schimmel te reconstrueren zagen ze dat de soort kan worden opgedeeld in vijf grote groepen of clades. Die zijn duizenden jaren lang los van elkaar geëvolueerd – te zien aan de vele mutaties – en vinden hun oorsprong op drie verschillende continenten.
Tegenwoordig spreken onderzoekers over de Zuid-Aziatische (die voornamelijk voorkomt in India en Pakistan), de Oost-Aziatische (Japan en Zuid-Korea), de Zuid-Amerikaanse (Colombia en Venezuela), de Zuid-Afrikaanse en de Iraanse clade. Alle isolaten buiten die regio’s – zoals die uit Europa, de VS en Australië – zijn terug te voeren tot reizigers die de schimmel uit de endemische gebieden meebrachten.
C. auris heeft zich de afgelopen tien jaar dus niet plots verspreid vanuit één land of continent. In werkelijkheid was de schimmel al duizenden jaren aanwezig in Azië, Afrika en Zuid-Amerika. Hoe komt het dan dat hij pas sinds 2009 frequent is gaan opduiken in ziekenhuizen?
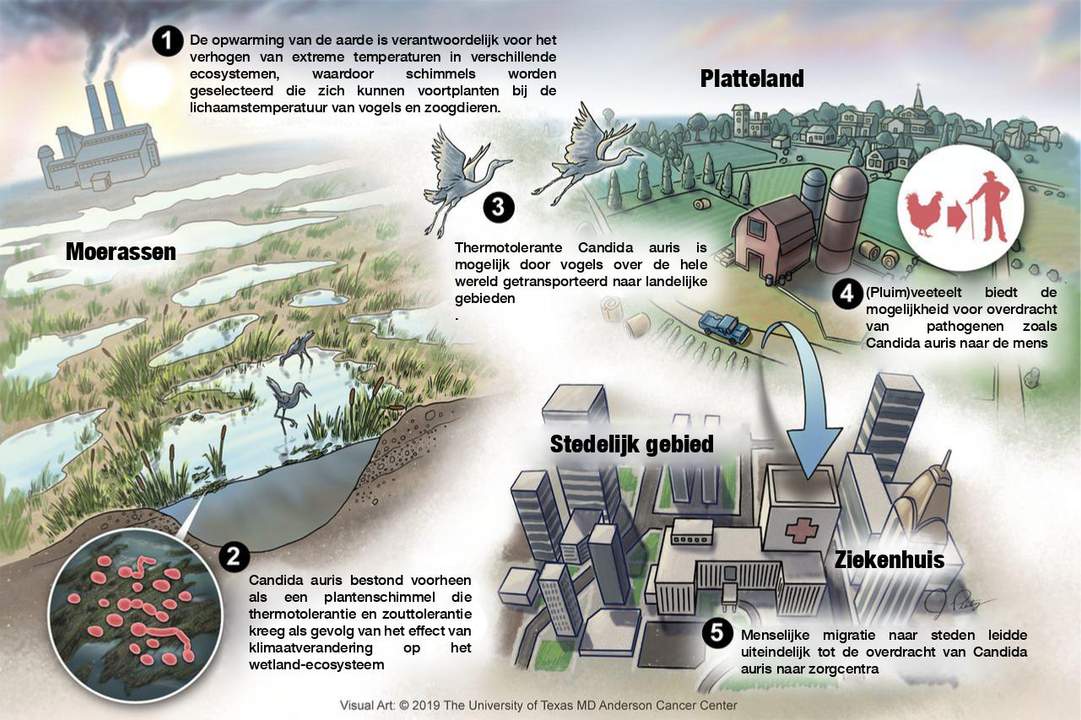
Uit onderzoek blijkt dat C. auris extreem tolerant is voor zout en hoge temperaturen, veel meer dan de meeste andere schimmels die mensen infecteren. Die vaststelling inspireerde een groep Amerikaanse onderzoekers om in 2019 een interessante hypothese te formuleren. C. auris zou oorspronkelijk een schimmel zijn geweest die leefde van dood plantaardig materiaal in brak- en zoutwatergebieden zoals mangroven en moerassen. Door de klimaatverandering zijn de temperaturen in die gebieden sterk gestegen. C. auris zou zich aan die extreme omstandigheden hebben aangepast. Dat moet het mogelijk hebben gemaakt om de zogeheten thermische barrière van warmbloedige dieren als vogels en zoogdieren te overschrijden.
De meeste vogels hebben een verhoogde lichaamstemperatuur tot 42°C. Het merendeel van de schimmelsoorten die verwant zijn aan Candida auris, zoals Candida haemuloni, groeien in omgevingen van maximaal 37°C: vogels kunnen zij dus niet besmetten. Maar C. auris, met zijn verhoogde weerstand, zou daartoe wel in staat zijn. Via vogels uit brak- en zoutwatergebieden kan de schimmel ook andere vogels hebben besmet. Waaronder soorten die dichter bij de mens staan, zoals pluimvee.
In de geschiedenis van epidemieën zijn zoönoses – ziektes die van dier op mens worden overgedragen – alomtegenwoordig. Je hebt bacteriële ziekteverwekkers, zoals de pest, en daarnaast zijn er virussen, zoals griep of SARS-CoV-2. Maar ook schimmels kunnen zoönoses zijn. Cryptococcus is bijvoorbeeld een erg dodelijke schimmel die wordt overgedragen van vogels naar mensen. Ons nauwe contact met dieren voor consumptie leidde al meermaals tot epidemieën met een zware tol voor de maatschappij. C. auris zou daarin niet anders zijn.
C. auris in het wild
Een C. auris-epidemie zou ineens ook de eerste zijn waarvan klimaatverandering mee aan de oorzaak ligt. Bewijzen voor de hypothese dat C. auris oorspronkelijk leefde in brak- en zoutwatergebieden bleven lang uit. Tot in maart, toen Indiase onderzoekers voor het eerst C. auris-isolaten uit de natuur aantroffen. Ze hadden onderzoek gedaan op de Andamanen, een afgelegen Indiase eilandengroep in de Golf van Bengalen tussen India en Myanmar. In sediment en in watermonsters van een toeristisch en een verlaten strand hadden ze C. auris gevonden.
De wilde, tropische habitat van de Andamanen is rijk aan mangrovevegetatie, die gedijt in brak water. Door deze vondst wint de hypothese van de Amerikaanse onderzoekers uit 2019 dus aan bewijskracht.
Elk van de 22 C. auris-isolaten van het toeristische strand zijn overigens multiresistent, terwijl de isolaten van het afgelegen strand dat niet zijn. Die laatste zijn ook minder tolerant voor hogere temperaturen. Dat kan erop wijzen dat C. auris van nature geen warmbloedige dieren of mensen treft en dat de schimmel zijn temperatuurtolerantie en resistentie pas ontwikkelde bij later contact met dieren, mensen en behandelingen met geneesmiddelen.
Ziekenhuisschimmel
We zijn het intussen al gewoon om bij het binnenkomen van de supermarkt: het handvat van de winkelkar te ontsmetten. Sommige micro-organismen, waaronder SARS-CoV-2 en Candida auris, kunnen uren of dagen overleven buiten het menselijk lichaam. C. auris is daar een extreem voorbeeld van: de schimmel kan weken overleven op allerlei materialen en oppervlaktes, zoals plastic en linnen. Dat stelt grote problemen, vooral in ziekenhuizen en woonzorgcentra.
Bovendien is C. auris ook nog eens erg tolerant voor heel wat ontsmettingsmiddelen die routinematig gebruikt worden bij het reinigen van kamers in zorginstellingen. In die mate zelfs dat een ziekenhuis in Brooklyn naast bedden, deurklinken en tafels ook het vals plafond en de vloer in een kamer moest vervangen om van Candida auris af te geraken, nadat een patiënt eraan was overleden. Dat soort volhardendheid is extreem uitzonderlijk voor een schimmel, en zelfs voor een micro-organisme in het algemeen.
Iedereen heeft weleens gehoord van de zogeheten ziekenhuisbacterie. Ze verspreidt zich bijzonder efficiënt in zorginstellingen, waar ze patiënten met open wonden, katheters of een verzwakt immuunsysteem besmet. Candida auris is de eerste schimmel ooit die zich op een vergelijkbare manier gedraagt. Daarom kan hij worden geclassificeerd als de eerste echte ‘ziekenhuisschimmel’.
Om van de schimmel af te geraken moest een ziekenhuis in Brooklyn naast bedden, deurklinken en tafels ook het vals plafond en de vloer vervangen
C. auris is erg goed in het koloniseren van de huid. De schimmel verspreidt zich zowel bij direct als indirect contact, via bijvoorbeeld de huid of de deurklink. In de Verenigde Staten heeft het CDC officiële aanbevelingen opgesteld om de verdere verspreiding te voorkomen in zorgcentra waar de schimmel voor het eerst opduikt. Naast een strikte handhygiëne en isolatie van besmette patiënten adviseert het CDC specifieke ontsmettingsmiddelen, zoals bleekwater.
De schimmel is voorts berucht om z’n ziekenhuisuitbraken. In België kon het Imelda-ziekenhuis in Bonheiden enkele jaren geleden een uitbraak in de knop breken. Elders, zoals in de VS, Spanje en het VK, is dat niet gelukt. Tientallen patiënten op de afdeling intensieve zorgen werden besmet. Een ware nachtmerrie, zeker als de unit ook nog eens overbevolkt zou blijken met covid-patiënten.
Dat gebeurde eind vorig jaar, toen de schimmel opdook in covid-afdelingen in onder meer Italiaanse, Braziliaanse, Indiase, Mexicaanse en Amerikaanse ziekenhuizen. Hoogstwaarschijnlijk droeg de schimmel op die manier bij tot het dodental van de huidige pandemie.
Opportunist
Ziekenhuizen zijn broeihaarden voor C. auris. De schimmel kan zich verspreiden tussen verzwakte patiënten of ongemerkt via zorgpersoneel of bezoekers die er zelf geen last van ondervinden. Zoals de meeste pathogene schimmels is C. auris namelijk een opportunist, wat betekent dat hij enkel infecties veroorzaakt wanneer zich daar de kansen toe voordoen. Denk aan vaginale Candida-infecties, meestal veroorzaakt door Candida albicans. Bij de meeste mensen maakt deze schimmel deel uit van de huid- en vaginale flora en is hij volstrekt onschadelijk. Maar als de natuurlijke microflora van de vagina uit balans geraken, kan er alsnog een infectie ontstaan.
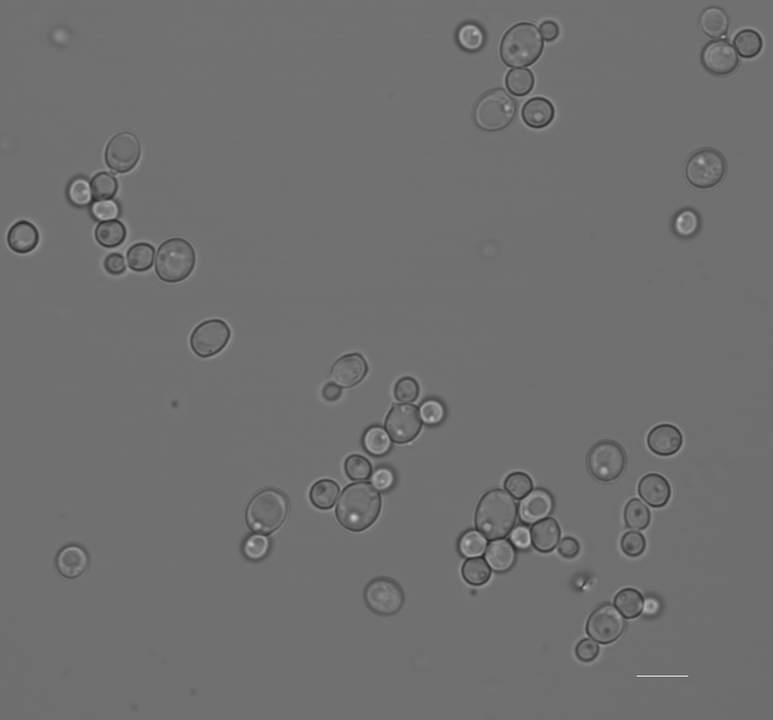
Meestal komen C. auris-infecties voor bij individuen met een verzwakt immuunsysteem. Risicopatiënten zijn prematuren, ouderen en zieken. Besmettingen kunnen zich ook voordoen na intensieve chirurgische ingrepen zoals transplantaties, bij auto-immuunziektes zoals aids of diabetes, of bij een lange hospitalisatie op intensieve zorgen. Ook voor ernstig zieke covid-patiënten stelt zich dus een risico.
Jaarlijks overlijden meer mensen aan schimmelinfecties dan aan borstkanker of malaria
De symptomen van een infectie lopen uiteen. Meestal krijgen patiënten te maken met aanhoudende koorts en koude rillingen. Maar omdat ze bijna altijd onderliggende ziektes hebben met vergelijkbare symptomen is het extreem moeilijk om op basis van die symptomen de diagnose te stellen van C. auris.
Pas na labtests kan een infectie worden bevestigd en de behandeling gestart. Al knelt daar meteen ook het schoentje. Er zijn maar weinig geneesmiddelen die je kunt inzetten tegen bloedinfecties van schimmels. C. auris blijkt er ook nog eens bijzonder resistent voor te zijn.
Een strijd met weinig wapens
Jaarlijks overlijden er meer mensen aan schimmelinfecties dan aan borstkanker of malaria. Toch hebben artsen maar drie soorten antischimmelmiddelen voorhanden om levensbedreigende bloedinfecties aan te pakken. Dat is bitter weinig als je weet dat er voor bacteriële infecties zo’n tiental antibioticaklassen beschikbaar zijn.
Schimmelinfecties worden nog steeds aangezien voor kwaaltjes. Nochtans eisen ze jaarlijks meer dan anderhalf miljoen doden
Dat er zo weinig medicijnen zijn, heeft verschillende redenen. Om te beginnen zijn schimmels eukaryote organismen, wat betekent dat hun celstructuur en metabolisme vergelijkbaar zijn met die van de mens. Bacteriën zijn dan weer prokaryoten. Zij hebben een simpelere structuur en een ander metabolisme. De enige goede doelwitten voor medicijnen zijn essentiële celprocessen of structuren die voldoende verschillen van onze eigen cellen. Als bijvoorbeeld een eiwit van een ziekteverwekker te veel lijkt op een eiwit in onze cel, dan zou het antibioticum of antischimmelmiddel ook die structuur doden en dus toxisch zijn voor ons lichaam.
Wat ook niet helpt, is dat schimmelinfecties nog steeds worden aangezien voor kwaaltjes. De meeste schimmelinfecties zijn inderdaad niet dodelijk, denk maar aan schimmelnagel of huiduitslag, vaginale infecties of spruw bij baby’s. Dat geeft schimmels een status als verwaarloosbare ziekteverwekkers. Niet enkel bij het brede publiek, maar ook bij de medische sector en bij het onderzoek naar nieuwe geneesmiddelen. Dodelijke bloedinfecties veroorzaakt door schimmels zijn dan wel veel zeldzamer vergeleken met deze veelvoorkomende kwaaltjes, ze eisen jaarlijks toch meer dan anderhalf miljoen dodelijke slachtoffers wereldwijd.
Tot slot zijn de antischimmelmiddelen die vandaag op de markt zijn wel degelijk werkzaam tegen de meeste infecties. De groep van echinocandines, op de markt sinds 2001, is bijvoorbeeld bijzonder effectief tegen Candida albicans, de meest voorkomende schimmel. Het is echter bij multiresistente schimmels als Candida auris dat het tekort aan nieuwe medicijnen angstaanjagend duidelijk wordt.
Resistentie tegen antischimmelgeneesmiddelen kan op verschillende wijzen tot stand komen. De meest gebruikelijke manier is wanneer een schimmel een DNA-mutatie krijgt die ervoor zorgt dat het doelwit van dat geneesmiddel lichtjes verandert. Het medicijn kan zijn werk niet meer naar behoren doen en de schimmel overleeft de therapie.
Het is bij multiresistente schimmels als deze dat het tekort aan nieuwe medicijnen angstaanjagend duidelijk wordt
Bij de meeste schimmels is multiresistentie zeldzaam. De combinatie van mutaties kan de schimmelcellen zodanig verzwakken dat ze geen infectie meer kunnen veroorzaken of in stand houden. Voor C. auris lijkt dat niet zo te zijn. Studies tonen aan dat tot 90 procent van alle C. auris-isolaten van patiënten resistent zijn tegen één geneesmiddel, terwijl tot wel 30 procent resistent is tegen twee en 4 procent resistent tegen de drie beschikbare geneesmiddelen. Bij deze laatste groep is zelfs een behandeling met een combinatie aan geneesmiddelen vaak niet meer effectief. Multiresistentie komt bij geen enkele andere pathogene schimmelsoort zo vaak voor als in Candida auris.
Uit alle macht voorkomen
In het laboratorium voor moleculaire celbiologie aan de KU Leuven onderzoeken mijn collega’s en ik hoe Candida auris resistent wordt. We gaan na hoe de schimmel meerdere mutaties kan combineren zonder aan virulentie te verliezen. Dat doen we door niet-resistente C. auris-isolaten in het lab gecontroleerd resistent te maken.
We maken daarbij gebruik van zogeheten experimentele evolutie: we laten cellen voortdurend opgroeien in de aanwezigheid van een antischimmelmiddel tot er een resistente mutatie optreedt. Daarna analyseren we het DNA van de resistente cellen om de mutaties te identificeren. Recent werden de eerste resultaten van ons onderzoek gepubliceerd in het wetenschappelijke tijdschrift mBio, waarin we nieuwe resistentiemechanismen aantonen.
Verder ontwikkelden we diagnostische methodes om C. auris en resistentiemutaties snel en goedkoop te kunnen detecteren in laboratoria en ziekenhuizen. Een ander team in ons lab houdt zich bezig met de zoektocht naar nieuwe antischimmelmiddelen.
Er moet nog veel werk gebeuren. Doordat de schimmel pas vrij recent werd ontdekt, staat het onderzoek nog in de kinderschoenen. Wetenschappers zijn wereldwijd druk in de weer met fundamenteel onderzoek naar de biologie van de schimmel. Anderen zoeken naar nieuwe antischimmelmiddelen of willen C. auris sneller kunnen detecteren en onschadelijk maken – bijvoorbeeld bij ziekenhuisuitbraken.
Hoewel C. auris aan een wereldwijde opmars bezig is, blijft het totale aantal besmettingen voorlopig laag. Het wordt geschat op ongeveer vijfduizend gevallen in meer dan 47 landen. Enkel patiënten met een sterk verzwakt immuunsysteem in bepaalde regio’s lopen risico op een besmetting. Onderzoeksfinanciering en de interesse van de farmasector zijn dan ook schaars.
Doordat de schimmel pas vrij recent werd ontdekt, staat het onderzoek nog in de kinderschoenen
Toch mogen we deze nieuwe schimmel niet negeren. Een toekomstige epidemie valt alleen te voorkomen als we onderzoek voeren naar hoe C. auris infecties veroorzaakt, hoe hij resistent wordt, hoe we hem kunnen doden en hoe we hem correct en snel kunnen identificeren. We moeten ons ervan bewust zijn dat deze schimmel op elk moment kan opduiken in onze geglobaliseerde samenleving. Wanneer dat gebeurt zijn een juiste en tijdige diagnose, correcte ziekenhuishygiëne en een gepaste behandeling van levensbelang.
Ten slotte moeten we stilstaan bij de manier waarop onze maatschappij sommige epidemieën in de hand werkt. Als de hypothese naar het ontstaan van Candida auris correct is, dan liggen klimaatverandering en contact met pluimvee aan de basis van het succes van deze schimmel. Net als SARS-CoV-2 zou C. auris het zoveelste voorbeeld vormen van een epidemie die we misschien hadden kunnen vermijden.



