De Nobelprijs Chemie 2019 gaat naar de ontwikkelaars van de lithium-ionbatterij.
John B. Goodenough (University of Texas), Stanley Whittingham (Binghamton University) en Akira Yoshino (Meijo University) delen de chemieprijs voor hun bijdrage tot de ontwikkeling van de lithium-ionbatterij, die mee aan de basis ligt van draadloze elektronica, elektrische wagens en opslag van hernieuwbare energie. ‘Lithium-ionbatterijen hebben de mensheid enorme voordelen gebracht’, aldus het Nobelprijscomité.
Toeval
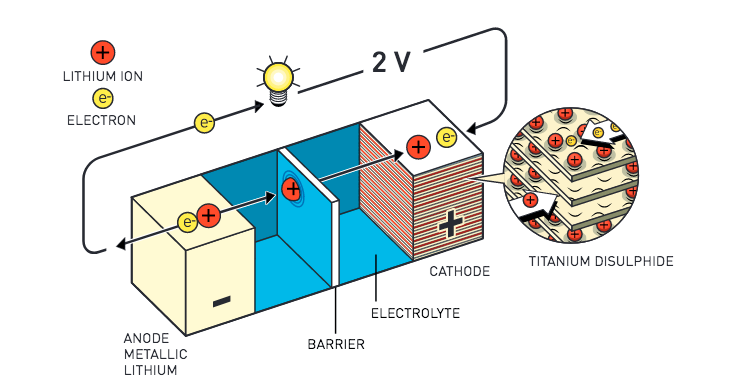
In de jaren 1970 bestudeerde Stanley Whittingham bij oliebedrijf Exxon supergeleidende materialen die op atomair niveau holtes bevatten waarin ionen (geladen deeltjes) zich kunnen vasthechten. Hij ontdekte zo hoe kaliumionen de geleidbaarheid van tantaaldisulfide beïnvloeden. Tot zijn verrassing stelde hij vast dat het resulterende materiaal erg energierijk was: het genereerde een spanning van een paar volt, beter dan veel van de toenmalige batterijen. Whittingham verlegde daarop de focus van zijn onderzoek van supergeleiders naar batterijen.
Tantaal heeft als nadeel dat het een zwaar element is – geen goede eigenschap als je het in een batterij wil verwerken. Whittingham slaagde erin het te vervangen door het lichtere titanium. In een batterij stromen elektronen van de negatief geladen anode naar de positief geladen kathode. De anode moet dus uit een materiaal bestaan dat makkelijke elektronen afstaat. Geen element doet dat liever dan lithium. Whittingham gebruikte het in de plaats van kalium en de eerste lithiumbatterij was een feit.
Oliecrisis
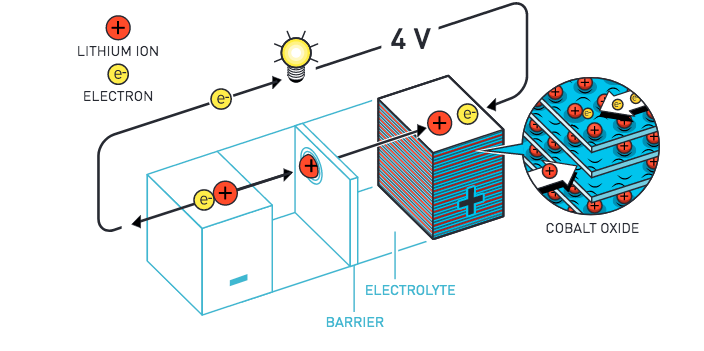
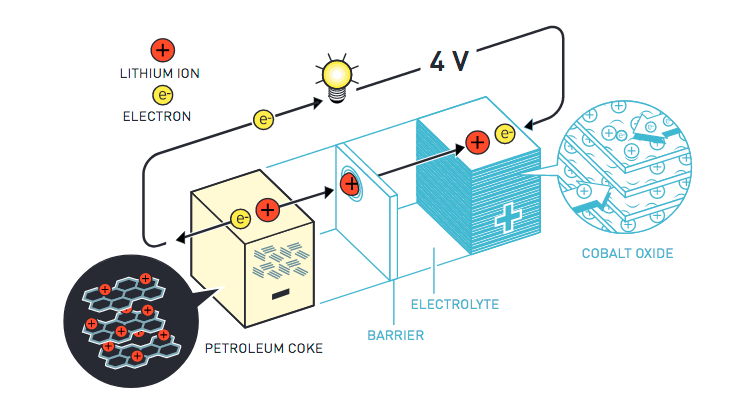
Net als Whittingham was John B. Goodenough aan het Massachusetts Institute of Technology (MIT) door de oliecrisis geïnteresseerd geraakt in alternatieve energiebronnen. Hij slaagde erin de batterij een hogere spanning te laten genereren, door voor de kathode kobaltoxide te gebruiken in plaats van titaniumdisulfide. Zo verdubbelde hij het voltage van 2 naar 4 volt. Akira Yoshino stelde de batterij verder op punt door voor de anode een combinatie van lithium en koolstof te gebruiken. Dat maakte de batterij krachtiger, veiliger en lichter.
Het grote voordeel van de lithium-ionbatterij zit hem in het feit dat ze niet werkt op basis van chemische reacties waarbij de elektroden afbreken, maar dankzij lithium-ionen die herhaaldelijk tussen de anode en kathode heen en weer kunnen reizen. Zo kan de batterij honderden keren worden opgeladen zonder dat ze minder goed gaat werken.
'Door hun werk hebben John Goodenough, Stanley Whittingham en Akira Yoshino de juiste condities gecreëerd voor een draadloze en fossielvrije samenleving’, vindt het Nobelprijscomité.



