Terwijl de lucht steeds droger wordt en de temperatuur daalt, is de jaarlijkse strijd tegen een schrale huid officieel begonnen. Een onderzoek van de Northwestern University heeft nieuw bewijs gevonden over de mechanismen die huidherstel en -vernieuwing regelen.
De buitenste laag van de huid, de epidermis, wordt voortdurend vernieuwd om dode of beschadigde cellen te vervangen. Elke maand worden we voorzien van een nieuw huidje. Maar hoe dit precies werkt, is nog niet helemaal duidelijk.
Om meer inzicht te krijgen in dit fenomeen, moeten we wat dieper in de moleculaire mechanismes van de huid kruipen. En dat is best taaie stof, hou je vast: het proces start met het kopiëren van het DNA in de cel, ook wel RNA-transcriptie genoemd. Dit kan vervolgens gebruikt worden als een sjabloon voor het maken van eiwitten met een specifieke functie. Dit sjabloontje bestaat uit zogeheten ‘intronen’ en ‘exonen’. Een intron is een stukje DNA dat in principe niet wordt gebruikt.
Je kunt het vergelijken met een boek waar willekeurige letters tussen de tekst staan. Deze willekeurige letters zullen in het uiteindelijke "boek" ertussenuit gehaald worden, waardoor een verhaal zal ontstaan dat volledig leesbaar is. De exonen vormen de leesbare tekst, en de intronen zijn dus vooral ‘genetische rommel’. Maar is dit echt wel zo?
Illustratie onder: Genen bestaan uit intronen en exonen. De productie van een eiwit start met het kopiëren van DNA naar RNA, gevolgd door het verwijderen van de intronen, en de vorming van het uiteindelijke eiwit die een specifieke rol gaat vervullen in de cel.
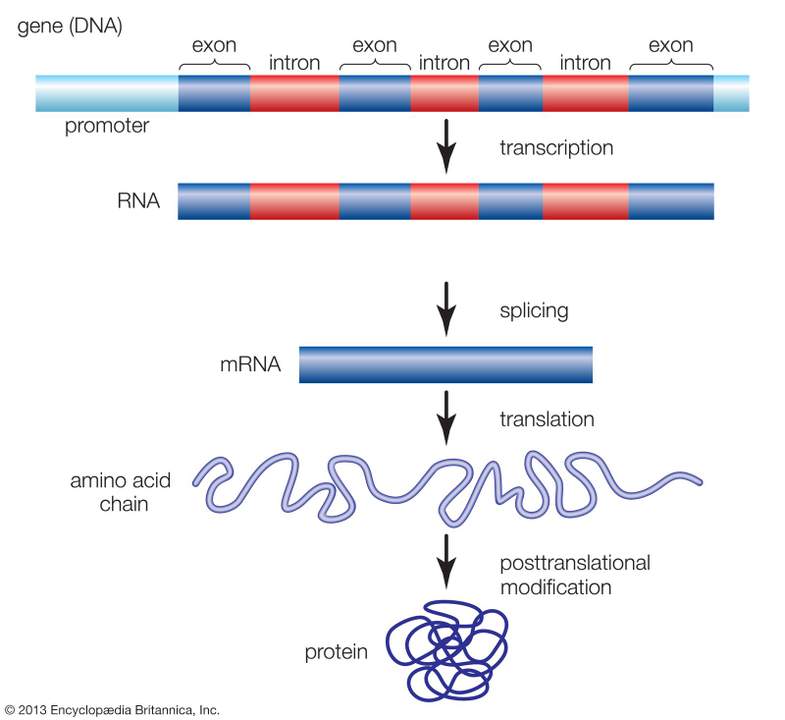
Intronen spelen in feite een cruciale rol bij het regelen van RNA-transcriptie gedurende de levensduur van een weefsel. Afhankelijk van waar transcriptie eindigt - in een intron of aan het einde van een gen - zal een epidermale stamcel ofwel een stamcel blijven of een gespecificeerde celbarrièrefunctie worden. Het team vond echter tegenstrijdige resultaten waarbij plekken gevonden zijn waar transcriptie eindigt - niet alleen aan het einde van een gen, maar vaak binnen een intron in het midden van een gen. En dit zou weleens voor meer herstelsystemen in ons lichaam kunnen gelden. Intronen moeten volgens de onderzoekers dus niet langer genegeerd worden.
Cellenpool achter de hand
Professor regeneratieve geneeskunde Martijn van Griensven: ‘Dit artikel is heel spannend. In het hele lichaam willen we een pool van cellen houden, die als basis voor herstel en vernieuwing gebruikt kunnen worden. Dit zijn de typische stamcellen of iets meer ontwikkelde progenitor cellen (deze cellen gaan dan al beetje een bepaalde richting op, zoals bijvoorbeeld huidcellen). Dit mechanisme is heel belangrijk voor alle situaties waar weefsel kapot gaat in het lichaam en moet herstellen, dat geldt niet alleen voor de huid. Denk bijvoorbeeld aan een botbreuk, waar ook stamcellen nodig zijn.’
‘Als we meer inzicht krijgen in hoe het herstelmechanisme precies werkt, dan kunnen we in situaties waar weefselregeneratie niet zo goed lijkt te werken ingrijpen in het proces en dit verbeteren. Natuurlijk is dat nog een lange weg, maar deze studie laat zien dat het mogelijk is. De keerzijde is wel, dat er ook tumoren kunnen ontstaan als we die basiscellen aanzetten en blijven delen. Dat moet gemonitord worden. Ons lichaam heeft gelukkig vaak meerdere wegen om iets te bereiken, zodat als er via een weg iets misgaat, het eventueel opgevangen kan worden door een andere weg.’
Bron: Nature Communications




