Antibioticaresistentie niet inperken of vertragen, maar met CRISPR-Cas volledig omkeren én dat verspreiden in een bacteriële populatie. Daarin slaagden wetenschappers van de UC San Diego (Californië, VS).
Genetische ingrepen om insectenpopulaties van bepaalde eigenschappen te ontdoen bestaan al langer dan een decennium. Zo zijn er al muggen gemaakt die het dodelijke malaria niet meer kunnen overdragen op mensen en die dat kenmerk heel efficiënt overdragen aan de volgende generatie muggen. Een soort genetisch populatiemanagement dus. Nu stellen Amerikaanse onderzoekers een gelijkaardig prototype voor dat antibioticaresistente bacteriën opnieuw antibioticagevoelig maakt en dat bovendien ook slim verspreidt in de bacteriepopulatie. De sleutels? Het revolutionaire CRISPR-Cas - en een bacteriële doorgeeftunnel.
In een eerste prototype uit 2019 maakten wetenschappers van de UC San Diego (Californië, VS) een genetische cassette (een aaneenschakeling van genen en andere DNA-elementen) die onder meer de instructies bevatte om het Cas9-enzyme te maken. Cas9 is een soort moleculaire schaar en een essentieel onderdeel van de bekende CRISPR-Cas technologie, waarmee wetenschappers kunnen knippen en plakken op precies gekozen plaatsen in DNA.
De taak die de Cas9-schaar in 2019 meekreeg was duidelijk: na introductie in de bacterie moest het knippen in het gen dat de bacterie antibioticaresistent maakt. Daarbovenop moest ook nog eens de volledige genetische cassette worden ingebouwd op diezelfde plaats, om zo het resistentie-gen volledig uit te schakelen. Het resultaat is een bacteriecel die weer gevoelig is aan het antibioticum in kwestie. Door enkele slimme stukjes in de cassette geeft de bacterie die eigenschap ook veelal door aan haar nakomelingen of dochtercellen. Dat noemen wetenschappers ‘verticale gentransfer’.
Enter 2026 en een verbeterd prototype ziet het licht. De onderzoekers breiden de genetische cassette uit met extra machinerie. Die stelt de bacteriecel nu ook in staat om haar eigen verworven, slimme genetische cassette door te geven aan niet-dochtercellen, zeg maar aan broers of zussen (of verre neven en nichten) - niet enkel aan nakomelingen. Dat noemt men horizontale gentransfer. Het verloopt via een ‘tunnel’ tussen twee bacteriën, een fenomeen dat bekend staat als ‘conjugatie’.
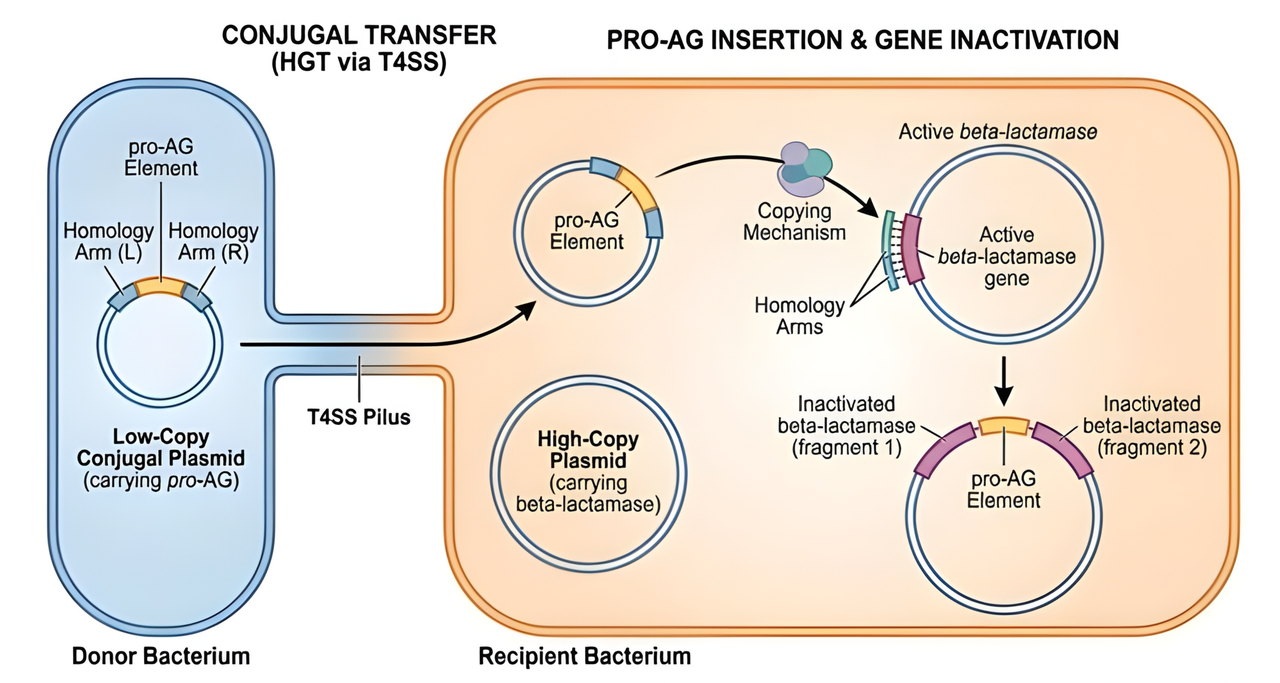
Belangrijk: horizontale gentransfer of conjugatie versnelt de verspreiding van de herboren antibiotica-gevoeligheid aanzienlijk doorheen de hele bacteriële populatie. De nieuwe techniek werkt bovendien ook voor de verspreiding van antibioticum-gevoeligheid in gevaarlijke bacteriële biofilms. Dat zijn slijmerige lagen van vele bacteriën op oppervlakken, bijvoorbeeld op een geïnfecteerd orgaan, wat veel complicaties met zich kan meebrengen.
Hoe moeten we de impact van dit systeem inschatten? Wel, de twintigste eeuw betekende de doorbraak van synthetische antibiotica. Zonder ingrijpen wordt de éénentwintigste eeuw echter een nefast kantelpunt voor dat sprookje. Door het onzorgvuldig en te frequent gebruik van antibiotica in de geneeskunde en landbouw ontstaan er steeds meer ‘superbacteriën’. Die zijn resistent tegen alle soorten antibiotica en kunnen dus niet bestreden worden. Zonder wetenschappelijke ingrepen zullen er in het jaar 2050 meer mensen sterven aan antibioticaresistente bacteriën dan aan kanker – meer dan tien miljoen patiënten per jaar.
De nieuwe techniek wil niet alleen antibioticaresistentie vertragen of de verspreiding ervan tegen gaan, maar het ook effectief ongedaan maken. Dat biedt volgens de wetenschappers meer voordelen dan bijvoorbeeld een breedspectrum antibioticum (een antibioticum werkzaam tegen veel verschillende soorten bacteriën). Zo’n one-fits-all antibioticum doodt immers ook goede bacteriën in je lichaam en versnelt zo de groei en dominantie van resistente bacteriën. Het nieuwe systeem dient momenteel als proof-of-concept en kan in de toekomst breed worden ingezet: van de gezondheidszorg en de landbouw tot omgevingsremediëring.



